Cuprins
- . scurt istoric şi utilizări
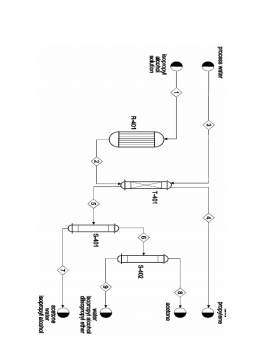
- 2.Locul şi rolul reactorului în schema tehnologică
- 2.1.Locul reactorului în instalaţie
- 2.2.Rolul reactorului
- 2.2.1.Termodinamica reacţiei
- 2.2.2.Calculul conversiei
- 2.2.1.Cinetica reacţiei chimice
- 3.Modelul fizic al reactorului
- 4.Modelul matematic al reactorului
- 4.1.Ecuaţiile modelului matematic al reactorului
- 4.2.Metode de rezolvare a modelului matematic
- 4.2.Programul de calcul
Extras din proiect
Acetona
1.Scurt Istoric
Acetona (dimetil cetona sau propanon),este un compus organic cu formula CH3-CO-CH3 este un lichid incolor cu miros caracteristic,fiind utilizat ca solvent organic pentru acetatul de celuloza,nitroceluloza si acetilena, dar si ca reactant intr-o serie de procese de termoliza si reactii de sinteza in chimia organica.Ea face parte din grupa cetonelor, caracteristic pentru strucutura acetonei este gruparea carbonilica de care se leaga dous grupari metil.Acetona se gaseste in cantitati mici in sangele uman si in urina.La diabetici continutul de acetone in urina este mai mare datorita descompunerii acidului acetoacetic.
Prima data a fost obtinuta in anul 1755 de Libavius prin distilarea uscata a acetatului de plumb.Natura si structura ei corecta a fost determinata in 1832 de catre Liebig si Dumas.Cererea tot mai mare de acetona a condus la dezvoltarea altor procedee bazate pe surse petroliere si in special propilena.Incepand din anul 1920, acetona s-a obtinut in special prin dehidrogenarea alcoolului isopropilic.Dupa 1953, o data cu aparitia procedeului de obtinere a fenolului prin oxidarea cumenului,acetona s-a obtinut ca co-produs alaturi de fenol.In 1961 s-a dezvoltat un nou procedeul de obtinere a acetonei din propilena.
Lichid incolor cu miros dulceag in concentratii mai ridicate intepator,usor inflamabil, in combinatie cu aerul formeaza un amestec explosiv. Se dizolva in orice proportii cu apa si majoritatea solventilor.
Utilizarea acetonei
Acetona este un bun solvent pentru cele mai multe materiale plastice si fibre sintetice, inclusiv cele utilizate in sticle de laborator realizate din polistiren, policarbonat si unele tipuri de polipropilena. Ea este folosită ca substanţă cu ajutorul căreia se extrage răşina, lipidele, uleiurile, colofoniul, acetatul de celuloză ca şi în cosmetică pentru înlăturarea lacului de pe unghii, in industria farmaceuti, ca agent de denaturare in alcoolul denaturat . In acetonă se dizolvă uşor gazul acetilenă.Ea mai este folosită în chimia organică în reacţiile de sinteză numite reacţii de aldoadiţie sau aldocondensare cu formare de alcool biacetonic C6H12O2 .Acetona cu apa oxigenată (H2O2) este folosită la obţinerea explosivului triacetatul de peroxid (APEX sau TATP). Este folosit ca o componentă volatilă a unor vopsele si lacuri. Acetona este, de asemenea, prezentă ca excipient în unele produse farmaceutice. Multe milioane de kilograme de acetonă sunt consumate în producţia de solvenţi de metil izobutil alcool şi izobutil metil cetona.
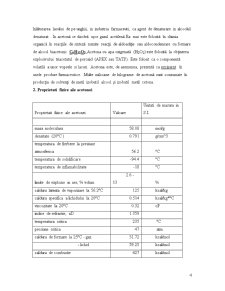
2. Proprietati fizice ale acetonei
Proprietati fizice ale acetonei Valoare Unitati de masura in S.I.
masa moleculara 58.08 mol/g
densitate (20ºC ) 0.791 g/cm^3
temperatura de fierbere la presiune atmosferica 56.2 ºC
temperatura de solidificare -94.4 ºC
temperatura de inflamabilitate -18 ºC
limite de explozie in aer, % volum 2.6 - 13 %
caldura latenta de vaporizare la 56.2ºC 125 kcal/kg
caldura specifica a lichidului la 20ºC 0.514 kcal/kg*ºC
viscozitate la 20ºC 0.32 cP
indice de refractie, nD 1.359
temperatura critica 235 ºC
presiune critica 47 atm
caldura de formare la 25ºC - gaz 51.72 kcal/mol
- lichid 59.25 kcal/mol
caldura de combustie 427 kcal/mol
entropia lichidului la 20ºC 47.82 kcal/mol*ºC
presiunea de vapori la 20ºC 179.6 mmHg
2.1 Metode de obtinere
Dehidrogenarea alcoolului isopropilic.Acest procedeu reprezinta cea mai importanta sursa de obtinere a acetonei si este folosit si in prezent.Exista mai multe variante ale acestui procedeu si anume:dehidrogenarea directa a alcoolului isopropilic sau oxidarea acestuia cu aer conform reactiilor:
CH3-CHOH-CH3 → CH3-CO-CH3 + H3 -16kcal/mol
CH3-CHOH-CH3 + 1/2O2 → CH3-CO-CH3 + H2O +42kcal/mol
Diferenta dintre aceste doua reactii consta in faptul ca, in primul caz se obtine ca produs secundar hidrigenul,iar in a doua reactie apa.
A.Oxidarea alcoolului izopropilic la acetona este o cale mai putin folosita, intrucat se obtin randamente mai scazute, iar pe de alta parte hidrogenul obtinut in procesul de dehidrogenare a alcoolului izopropilic este un produs valoros, care contribuie la reducerea costurilor de fabricatie ale acetonei.Reactie de oxidare are loc intr-un reactor ca cel de la dehidrogenare si se face la temperaturi mai ridicate 500-600ºC , consumul de combustibil este asemanator, intrucat reactie este exoterma.Drept catalizator se utilizeaza cupru metalic sau argint. Faza lichida constituita din acetona bruta este supusa purificarii prin distilare.
B.Oxidarea alcoolului izopropilic la acetona poate decurge si pe alta cale,prin hidroxihidroperoxid de propan.Reactia are loc la temperatura de 95-140ºC si presiune de 3 at intr-un reactor tip coloana, in care alcoolul izopropilic proaspat si recirculat se introduc pe sus, iar oxigenul este alimentat pe la partea inferioara.Reactia este exoterma, preluarea caldurii de reactie facandu-se prin refluxarea acetonei si alcoolului izopropilic.
C.Din alcoolul izopropilic, acetona se mai poate obtine printr-o reactie de transhidrogenare, care converteste acroleina la alcool alilic:
CH2=CH-CHO + CH3-CHOH-CH3 → CH2=CH-CHOH + CH3-CO-CH3
Reactia are loc in faza de vapori la temperaturi ridicate (circa 400ºC ) si presiuni moderate (2-4 at ), in prezenta de oxid de magneziu si oxid de zinc pe suport de silice.Pentru a mari conversia in alcoolul alilic se foloseste un exces mare de alcool izopropilic.
Preview document
Conținut arhivă zip
- Proiect Reactoare - Obtinere Acetona din Alcool Izopropilic.doc