Extras din proiect
Ni+C Ni+CO
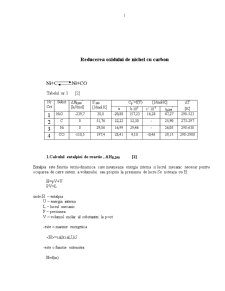
Tabelul nr.1 [2]
Nr
Crt Subst Hf,298
[kJ/mol] S 298
[J/mol K] Cp =f(T) [J/mol K] T
a b 103 c’ 10-5 cp298 [K]
1 NiO -239,7 38,0 -20,88 157,23 16,28 47,27 298-523
2 C 0 51,76 22,22 12,30 - 25,90 273-297
3 Ni 0 29,86 16,99 29,46 - 26,05 298-630
4 CO -110,5 197,4 28,41 4,10 -0,46 29,15 298-2900
1.Calculul entalpiei de reactie , HR,298 [1]
Entalpia este functia termodinamica care insumeaza energia interna si lucrul mecanic necesar pentru ocuparea de catre sistem a volumului sau propriu la presiunea de lucru.Se noteaza cu H.
H=pV+U
PV=L
unde:H – entalpia
U – energia interna
L – lucrul mecanic
P – presiunea
V – volumul molar al substantei la p=ct
-este o marime energetica
H =cal,kcal,J,kJ
-este o functie extensiva
H=f(m)
Formula de calcul:
HR,298 = i fp,298 - j Hfr,298
unde: HR,298 - entalpia standard de reactie la presiunea p=1atm si temperatura T=298K
i, j – coeficienti stoechiometrici ai reactantilor respectiv ai produsilor de reactie
Hfp,298 – entalpia de formare a produsilor de reactie la presiunea p=1atm si temperatura T=298K
Hfr,298 – entalpia de formare a reactantilor la presiunea p=1atm si temperatura T=298K
HR,298 = i Hfr,298 - j Hfr,298 =[1mol * 0+1mol(-110,5)kJ mol] –
– [1mol(-239,7)kJ mol+1mol * 0]= - 110,5kJ+239,7kJ=129,2kJ.
HR,298 =129,2 kJ
Daca HR,298 0 , reactia este endoterma .
2.Aprecieri asupra stabilitatii compusilor obtinuti in comparatie cu alti compusi similari ai aceluiasi element.
In cazul substantei cu entalpia de formare pozitiva ( H=129,7 kJ) , substanta cea mai stabila este substanta pentru care entalpia de formare standard este mai indepartata de zero pe axa pozitiva .
3.Calculul entropiei de reactie SR,298 [1]
Entropia reprezinta o masura a gradului de dezordine interna a unui sistem . Se noteaza cu S si a fost introdusa in calculul termodinamic de principiul al doilea al termodinamicii .
Preview document
Conținut arhivă zip
- Reducerea Oxidului de Nichel cu Carbon.doc