Cuprins
- Tema de proiect 4
- 1. Procedee de fabricare 5
- 1.1 Metode de sinteză chimică 6
- 1.1.1 Hidratarea catalitică directă a etilenei 6
- 1.1.2 Hidratarea catalitică indirectă a etilenei 8
- 1.1.3 Hidrocarbonilarea metanolului 10
- 1.1.4 Carbonilarea metanolului sau a metil acetatului 11
- 1.2 Metode de obţinere prin biosinteză 12
- 2. Justificarea procedeului ales 16
- 3. Aspecte privind reacţia de biosinteză 17
- 4. Descrierea procesului tehnologic 19
- 5. Materii prime şi auxiliare 23
- 5.1 Materii prime 23
- 5.2 Materiale auxiliare 25
- 6. Produse finite şi secundare 26
- 7. Bilanţ de materiale 27
- 7.1 Schema operaţiilor principale 29
- 7.2 Bilanţ de materiale pe faza de fluidificare 30
- 7.3 Bilanţ de materiale pe faza de zaharificare 31
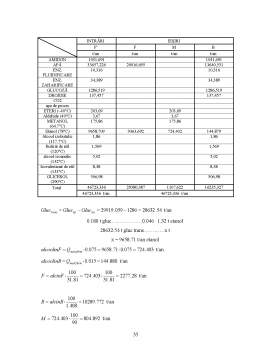
- 7.4 Bilanţul de materiale pe faza de fermentare 32
- 7.5 Bilanţ pe faza de distilare 34
- 7.6 Bilanţ pe faza de rectificare 36
- 8. Bilanţul termic 37
- 8.1 Bilantul termic pentru operaţia de fluidificare 37
- 8.2 Bilanţul termic pe faza de răcire după fluidificare 38
- 8.3 Bilanţul termic pe faza de zaharificare 38
- 8.4 Bilanţul termic pe faza de răcire după zaharificare 38
- 8.5 Bilanţul termic pe faza de fermentaţie 39
- 8.6 Bilanţul termic pe coloana de distilare 40
- 8.7 Bilanţul termic pe coloana de rectificare 41
- 8.8 Bilanţul termic pe fierbătorul de la baza coloanei de rectificare 42
- 9. Consumuri specifice 42
- 10. Efluenţi industriali 43
- 11. Dimensionarea de proces a principalelor utilaje 44
- 11.1.1 Dimensiunile geometrice ale bioreactorului tip autoclavă 44
- 11.1.2 Determinarea duratei de fermentare 44
- 11.1.3 Determinarea numărului de reactoare necesare 46
- 11.1.4 Bioreactorul de fermentaţie 47
- 11.1.5 Verificarea bioreactorului la transfer termic 53
- 11.2 Dimensionarea de proces a preincălzitorului coloanei de rectificare 58
- 11.2.1 Bilanţul termic pe schimbător 58
- 11.2.2 Determinarea suprafeţei de transfer termic 59
- 11.2.3 Exemplu de calcul pentru αabur 60
- 11.2.4 Exemplu de calcul pentru αamestec 60
- 11.2.5 Alegerea geometriei schimbătorului 61
- 11.2.6 Verificarea coeficientului total de transfer termic 61
- 11.2.7 Verificarea suprafeţei de transfer termic 61
- 11.2.8 Calculul racordurilor geometrice 62
- 12. Elemente de masură şi reglare 63
- 13. Protecţia muncii 64
- 14. Calculul tehnico-economic 67
- 15. Bibliografie 70
Extras din proiect
Tema de proiectare
Să se proiecteze o instalaţie de obţinere a alcoolului etilic din porumb, prin proces enzimatic, cu următoarele date iniţiale:
- producţia impusă: 8620 t/an;
- fondul anual de timp: 7200 h / an;
- materia primă: amidon din porumb;
- microorganism utilizat: Saccharomyces cerevisiae;
- concentraţia iniţială de substrat: CS0 = 250 g / l;
- concentraţia iniţială de celule: CX0 = 1 g / l.
1. Procedee de fabricare
Etanolul sau alcoolul etilic, este cunoscut şi sub denumirea de spirt, alcool cereal, alcool absolut sau etil hidrat. În funcţie de procentul de apă conţinut, de modul de preparare precum şi de utilizarea lui, există mai multe sortimente pe piaţă. Alcoolul de puritate 99%, deseori denumit alcool absolut, este folosit cu precădere în industria farmaceutică, fie la prepararea tincturilor, fie la extragerea principiilor active din diferite plante. Etanolul se mai foloseşte ca solvent şi conservant, ca antiseptic, precum şi în industria parfumurilor.
Alcoolul etilic este un component important din băuturile alcoolice, acestea fiind obţinute prin fermentarea carbohidraţilor. Plămada fermentată poate constitui o băutură în sine, cum e cazul berii sau a vinului, sau poate fi supus operaţiilor de purificare, caz în care se obţin produse spirtoase cu conţinut ridicat de alcool.
Dacă alcoolul este foloşit în alte scopuri decât alimentare, atunci acesta este impurificat cu metanol, piridină, formaldehidă, etc. Acesta poate fi folosit apoi în industrie ca solvent, materie primă pentru sinteza altor compuşi sau drept combustibil.
Scurt istoric
Etanolul poate fi conşiderat unul din cele mai vechi alimente cunoscute omului. Berea fermentată se consuma în Babilon, iar vinul a fost produs încă din anul 3000 î.e.n.
Procesul de distilare îşi are originile prin secolul X – XIV. În acestă vreme s-a descoperit şi efectul “spiritual” al alcoolului de unde i s-a dat şi numele spiritus. Primele distilerii au avut ca scop obţinerea alcoolului pentru scopuri medicinale.
Până în secolul XVII s-a considerat că fermentaţia alcoolică este un proces rezidual, în care drojdia rezultată era aruncată. Natura fermentaţiei a fost clarificată în secolul 19 odată cu descoperirea microscopului, când s-a dovedit că celulele de drojdie sunt organisme vii. Totuşi a durat 150 de ani până când s-a recunoscut că organisme vii sunt responsabile pentru procesul de fermentaţie.
În secolul 19 au apărut două teorii menite să explice obţinerea etanolului. Una dintre ele este teoria “vitală” promovată de Louis Pasteur (1822-1895), conform căreia organismele vii sunt responsabile pentru transformarea zaharurilor în alcool. A doua teorie este cea “mecanică” elaborată de Justus Freiherr Von Liebig (1803-1873) şi Friedrich Wöhler (1800-1882). O dovadă menită să susţină teoria “mecanică”, prin care un proces fizico-chimic conduce la conversia zaharului în etanol a venit de la Edward Buchner (1860-1917), care a demonstrat că fermentaţia alcoolică este realizată de o substanţă din plămadă, nu de celula de drojdie în sine. Această substanţă a fost mai târziu identificată ca fiind o enzimă. La ora actuală se cunoaşte că, în final, enzimele sunt responsabile pentru transformarea complexă a glucidelor în etanol.
1.1 Metode de obţinere prin sinteză chimică
Obţinerea etanolului din etilenă prin reacţia cu acid sulfuric a fost realizată acum 100 de ani. Producţia la scară industrială a alcoolului etilic a fost pusă la punct în anii 1930 de către compania Carbide and Chemical Corporation. Precesul presupunea absorbţia etilenei în acid sulfuric şi apoi scindarea hidrolitică a etil sulfatului rezultat. Acest procedeu a fost ulterior înlocuit cu hidratarea catalitică directă a etilenei introdusă de Shell Chemical Compan în anul 1948.
Modalităţi mai recente de sinteză se bazează pe materii precum metanol, gaz de sinteză, etc.
1.1.1 Hidratarea catalitică directă a etilenei
Chimia reacţiei
Pe intervalul de temperatură în care se desfăşoară reacţia, hidratarea etilenei la etanol funcţionează dupa o reacţie reversibilă controlată de echilibrul:
C2H4 (g) + H2O (g) ↔ C2H5OH (g) H = - 43.4 kJ (1.1)
În condiţiile normale din reactor (aproximativ 250-300 °C, 5-8 MPa, debit echimolar etilenă-apă), conversia la echilibru a etilenei este de 7 - 22%. O temperatură mai scăzută în reactor favorizează conversia etilenei, dar în aceste condiţii mai apare încă o reacţie de echilibru, formarea dietieterului conform reacţiei (2):
C2H5OH + C2H4 ↔ C2H5OC2H5 (1.2)
La presiuni mai mari etilena polimerizează cu formare de butene sau olefine care sunt apoi transformate în alcooli superiori.
Preview document
Conținut arhivă zip
- Instalatie de Obtinere a Alcoolului Etilic din Porumb prin Fermentatie.doc