Cuprins
- Consideratii teoretice 3
- Spectroscopia de emisie atomică 3
- Spectroscopia de emisie atomică în flacără 5
- Spectroscopia de emisie atomică cu plasmă 6
- Spectrometria de emisie atomică cu plasmă cuplată inductiv 6
- Spectroscopia de emisie atomică cu plasmă cuplată 8
- inductiv și spectrometru de masă (IPC-MS) 8
- Spectroscopia de emisie atomică cu plasmă de 8
- microunde (MPT-AES) 8
- Spectroscopia de emisie atomică descărcare electrică 9
- cu scânteie sau cu arc 9
- Aparatură 9
- Spectrometre și fotometre 9
- Spectrometre cu reţea de difracţie 11
- Generatorul de înaltă frecvență 12
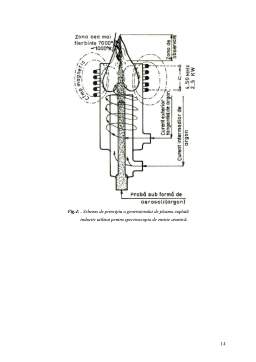
- Generatorul de plasmă cuplată inductiv 13
- Bibliografie 15
Extras din proiect
Consideratii teoretice
Spectroscopia este o denumire generică dată unei clase de procedee şi tehnici experimentale prin care se urmăreşte şi se cuantifică efectul emisiei sau absorbţiei de energie de către o probă solidă lichidă sau gazoasă în scopul analizei calitative şi/sau cantitative a acesteia. În urma acestor interferenţe energetice rezultă spectre ce reprezintă distribuţii ale intensităţii unei radiaţiei în funcţie de lungimea de undă, de frecvenţă (energie), de masă, iar in cazul particulelor grele, în funcție de viteză.
Spectrometrul este mijlocul tehnic prin care se materializează diferitele metode și tehnici spectroscopice. Spectrometrul, în înțelesul cel mai larg, este un instrument optic sau optoelectronic dispersiv destinat analizei spectroscopice calitative și antitative și este format dintr-o prismă sau o reţea de difracție, fante optice şi un detector fotoelectric pentru a măsura transmitanţa sau absorbanţa. La ora actuală, termenul de spectrometru este aplicat şi la mijloacele de măsurare nedispersive echipate cu interferometre, prelucrarea datelor făcîndu-se prin Transformată Fourier. Dat fiind faptul că spectroscopia şi aparatura spectroscopică au evoluat continuu de-a lungul anilor și terminologia folosită s-a diversificat.
Spectroscopia de emisie atomică
Analiza colorării flăcării. Analiza vizuală a colorării flăcării este o metodă rapidă şi ieftină folosită pentru identificarea elementelor chimice încă de la începuturile chimiei şi folosită şi astăzi în chimia analitică. Principiul constă în compararea spectrului vizibil (al culorii) emis de o probă, excitată intr-o flacără, cu diferite spectre luminoase ale unor elemente cunoscute. Cu toate că intensitatea emisiei luminoase a probei aduse în flacără este proporţională cu concentraţia elementului sau ionului, în substanţa de analizat este greu să se facă aprecieri ale concentraţiei pe calea analizei vizuale a emisiei luminoase. Explicaţia ştiinţifică a fenomenului de emisie atomică constă în modificarea raporturilor energetice ale straturilor electronice exterioare a atomilor sub influența aportului de energie termică dat de flacără. Electronii exteriori (electronii de valenţă) ai unui atom pot fi deplasaţi prin aport de energie (în acest caz energie termică de la flacără) pe straturi enegetice mai îndepărtate de nucleul atomului, neocupate de alţi electroni, unde ei se vor găsi într-o aşa zisă stare excitată. Aceşti electroni posedă o energie potenţială ridicată, iar la fluctuaţii ale aportului de energie termică, sau la încetarea acestuia, ei revin pe stratul electronic de unde au plecat şi emit energia excedentară sub forma unui foton de o anumită lungime de undă (o anumită culoare). Revenirea pe nivelul energetic de bază se poate face şi în trepte. La parcurgerea fiecărei trepte de la un nivel energetic superior către un nivel energetic inferior se emite radiaţie luminoasă de o anumită culoare. Energia luminoasă emisă depinde de diferenţa nivelului energetic ΔE. Această diferenţă caracterizează fiecare element. Energia fotonilor determină lungimea de undă λ şi prin aceasta culoarea emisă de către element sau ion:
ΔE=h =h.f
Unde: c - viteza luminii;
h - constanta lui Plank.
Atunci când un anumit element prezintă o colorare a flăcării şi majoritatea ionilor lui din combinaţi chimice prezintă de regulă aceeaşi coloraţie a flăcării. Există şi excepţii, aşa de exemplu sulfatul de bariu prezintă o culoare verde a flăcării pe când fosfatul de bariu nu prezintă colorare a flăcării. Multe elemente emit la temperaturi ridicate linii spectrale vizibile.
Pentru elemente mai greu excitabile sunt necesare surse energetice mai puternice decât flacăra
de gaz precum arcul electric, plasma, laserul, aparatura de analiză fiind în aceste cazuri mai complexă. Odată cu dezvoltarea analizei instrumentale, tehnicile de analiză ale radiaţiei luminoase specifice emisă de elemente şi ioni au trecut de la analiza vizuală cu ochiul şi creierul, la analiză spectroscopică. Cu ajutorul spectroscopiei se pot localiza mult mai bine poziţiile radiaţiilor emise pe scara lungimilor de undă şi prin aceasta identificarea calitativă precisă a elementelor. De asemenea, prin măsurători fotometrice efectuate pe anumite segmente specifice ale spectrului (linii sau benzi) se poate determina concentraţia elementului sau ionului din intensitatea emisiei luminoase.
Preview document
Conținut arhivă zip
- Spectroscopia de Emisie.doc